Resonancias y Sistemas Aromáticos☝
Aromáticos
Son derivados monosustituidos del benceno y se nombran de la misma forma que otros hidrocarburos pero usando benceno como nombre padre.
- Si los sustituyentes del benceno son pequeños (6 átomos de carbono o menos) el compuesto se nombra como un benceno sustituido.
- Si el sustituyente tiene más de 6 átomos de carbono, el benceno se considera un radical y se nombra como fenil.
Formas de representar al benceno.


 |  |  |
bromobenceno | nitrobenceno | metilbenceno |
- Bencenos disustituidos: Si el anillo de benceno tiene 2 sustituyentes, se indica su posición mediante los números 1,2 (posición orto), 1,3 (posición meta) o 1,4 (posición para), teniendo el número 1 el sustituyente más importante.
 |  |  |
| 1,2-dimetilbenceno | 1,3-dimetilbenceno | 1,4-dimetilbenceno |
| orto- dimetilbenceno | meta- dimetilbenceno | para- dimetilbenceno |
| o– dimetilbenceno | m– dimetilbenceno | p– dimetilbenceno |
- Si el anillo de benceno tiene más de 2 sustituyentes se numeran de manera que se asigne los menores localizadores. En caso de que las opciones sean iguales, use el criterio del orden alfabético.

1-etil-2,3-dimetil-4-propilbenceno

5-etil-1,9-difenil-2-metilnonano
 |  |
4-bromo-1,2-dimetilbenceno | 1-cloro-2,4-dinitrobenceno |
Compuestos aromáticos policíclicos
 |  |  |
Propiedades Físicas
- Son compuestos de baja polaridad.
- • Insolubles en agua
- • Menos densos que el agua
• Hasta no hace mucho y a pesar de su inflamabilidad, el benceno se usó ampliamente como disolvente. Este uso ha desaparecido prácticamente una vez que fue demostrado que el benceno es un cancerígeno. El tolueno ha reemplazado al benceno como disolvente orgánico barato, porque tiene propiedades similares como disolvente y no se ha demostrado que sea cancerígeno en los sistemas celulares y a los niveles que lo es el benceno.
Propiedades Químicas del Benceno
Sufre reacciones típicas de Sustitución electrofílica como la halogenación, nitración, sulfonación y alquilación.
• Las reacciones de adición, como la hidrogenación, se producen solo en presencia de catalizadores y a alta temperatura.
Resonancia
La resonancia (denominada también mesomería) es una herramienta empleada (predominantemente en química) para representar ciertos tipos de estructuras moleculares. La resonancia consiste en la combinación lineal de estructuras teóricas de una molécula (estructuras resonantes o en resonancia) que no coinciden con la estructura real, pero que mediante su combinación nos acerca más a su estructura real. El efecto es usado en una forma cualitativa, y describe las propiedades de atracción o liberación de electrones de los sustituyentes, basándose en estructuras resonantes relevantes, y es simbolizada por la letra R o M (a veces también por la letra K). El efecto resonante o mesomérico es negativo (-R/-M) cuando el sustituyente es un grupo que atrae electrones, y el efecto es positivo (+R/+M) cuando, a partir de la resonancia, el sustituyente es un grupo que dona electrones.
- Ejemplos de sustituyentes -R/-M: acetilo - nitrilo - nitro
- Ejemplos de sustituyentes +R/+M: alcohol - amina
La resonancia molecular es un componente clave en la teoría del enlace covalente. Para su existencia es imprescindible la presencia de enlaces dobles o triples en la molécula. El flujo neto de electrones desde o hacia el sustituyente está determinado también por el efecto inductivo. El efecto mesomérico como resultado del solapamiento (traslape) de orbitales p (resonancia) no tiene efecto alguno en este efecto inductivo, puesto que el efecto inductivo está relacionado exclusivamente con la electronegatividad de los átomos, y su química estructural (qué átomos están conectados a cuáles).
Numerosos compuestos orgánicos presentan resonancia, como en el caso de los compuestos aromáticos.
Conjugación
La conjugación existe en otras estructuras diferente a la de enlaces covalentes simples y dobles alternados. Mientras existan átomos contiguos en la cadena que posean un orbital p, el sistema puede ser considerado conjugado. Por ejemplo el furano, mostrado a la derecha, es un anillo de cinco miembros con dos dobles enlaces alternados y un átomo de oxígeno en la posición 1. El átomo de oxígeno tienes dos pares libres, uno de los cuales ocupa un orbital p en dicha posición, manteniendo la conjugación del anillo de cinco miembros. La presencia de un átomo de nitrógeno en el anillo, o de grupos en posiciones α del anillo tal como un grupo carbonilo (C=O), un grupo imina (C=N), un grupo vinilo (C=C), o un anión puede bastar como una fuente de orbitales p para mantener la conjugación.
Hibridación y estructuras de resonancia
La molécula de benceno, de fórmula C6H6, es una molécula cíclica plana cuya estructura de Lewis se puede representar como:
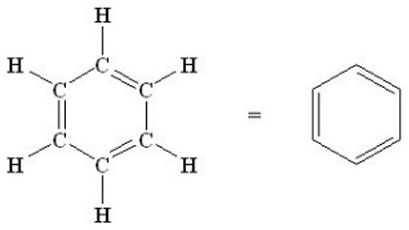
Como vemos, según esta representación, tendría 3 enlaces dobles carbono-carbono y tres enlaces simples. No obstante, experimentalmente se sabe que, en efecto, la molécula de benceno es plana, los ángulos son de 120º y los 6 enlaces carbono-carbono son idénticos y presentan propiedades intermedias entre un enlace doble y un enlace simple, siendo la distancia de enlace de 0,142 nm (la de un enlace simple es de 0,152 nm y la de un enlace doble de 0,134 nm). Por este motivo, el benceno se suele representar como:
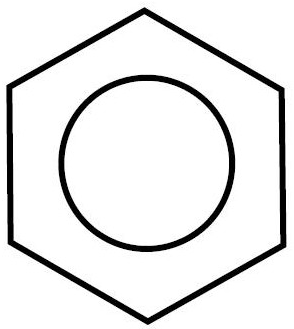
Omitiendo, además, los átomos de hidrógeno. Esto indica que es un híbrido de resonancia, una «mezcla» entre dos estructuras posibles (puedes ver el vídeo sobre mesomería o resonancia):
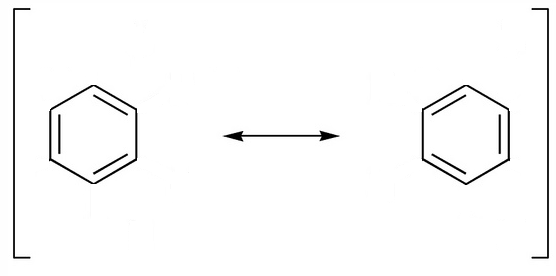
El benceno presenta unas características propias distintas a los alcanos y alquenos, y que recibe el nombre de carácter aromático o aromaticidad. El hecho de que la molécula sea plana, los ángulos de 120º y todos los enlaces iguales, se puede justificar considerando una hibridación sp2 de los 6 átomos de carbono, pero con enlaces pi deslocalizados. Es decir:
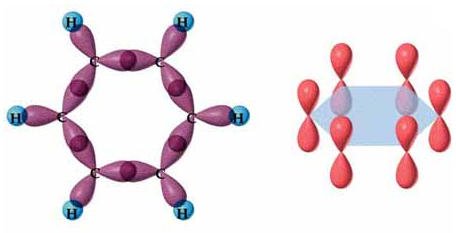
Como se puede observar, cada átomo de carbono tiene 3 orbitales híbridos sp2 colocados en un plano y dirigidos a los vértices de un triángulo equilátero, y un orbital p sin hibridar, semiocupado, perpendicular al plano de los híbridos. En total la molécula tiene 6 orbitales p que solaparán entre sí lateralmente, formando un sistema de enlaces pi deslocalizados, es decir, la densidad electrónica se distribuye de forma simétrica por encima y por debajo del plano:
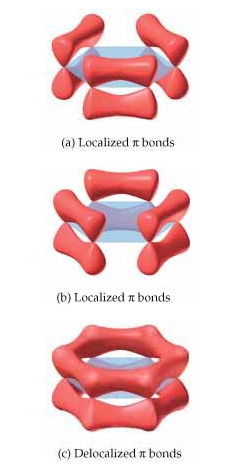
En la imagen de pueden ver lo que serían los enlaces localizados, tal y como se podía plantear en las dos estructuras resonantes del benceno, y la realidad, en la que se trata de 6 enlaces intermedios simple-doble, los llamados enlaces pi deslocalizados.
A continuacion se te presentara diferentes videos que pueden ayudar a entender de mejor manera las estructuras resonantes:Estructuras resonantes para el benceno y el anión fenóxido y Benceno, estructura y resonancia
Aromaticidad
En química orgánica, la aromaticidad describe la resonancia de los dobles enlaces conjuntados en moléculas cíclicas. Gracias a esta resonancia, los electrones de los dobles enlaces quedan deslocalizados en todo el anillo, lo que mejora la estabilidad y permite que las moléculas adquieran una geometría plana.
Los compuestos aromáticos más habituales derivan del benceno, por lo que a veces se usa como sinónimo, aunque existen muchos más tipos.
La aromaticidad se define como una propiedad de los cicloalquenos conjugados, también llamados arenos o hidrocarburos aromáticos, por la cual presentan una estructura plana y alta estabilidad respecto a moléculas con una disposición atómica similar pero sin la presencia de dobles enlaces conjugados.
Los dobles enlaces conjugados son los dobles enlaces que aparecen de forma alterna a lo largo de una cadena de átomos de carbono, pero en realidad los electrones de los dobles enlaces conjugados no están comprometidos a átomos de carbono concretos de la molécula, sino que se encuentra deslocalizados.
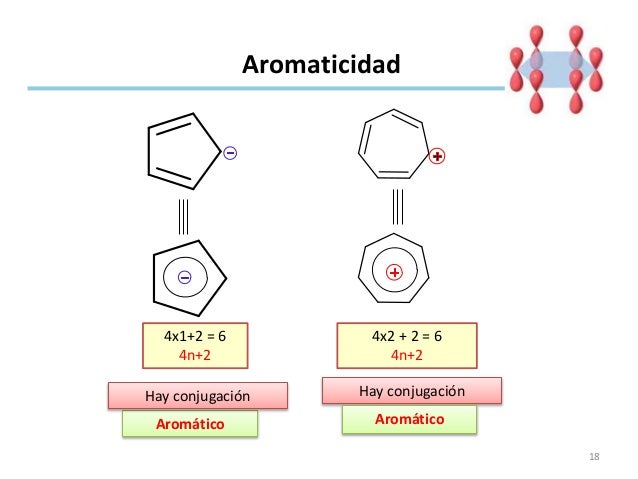
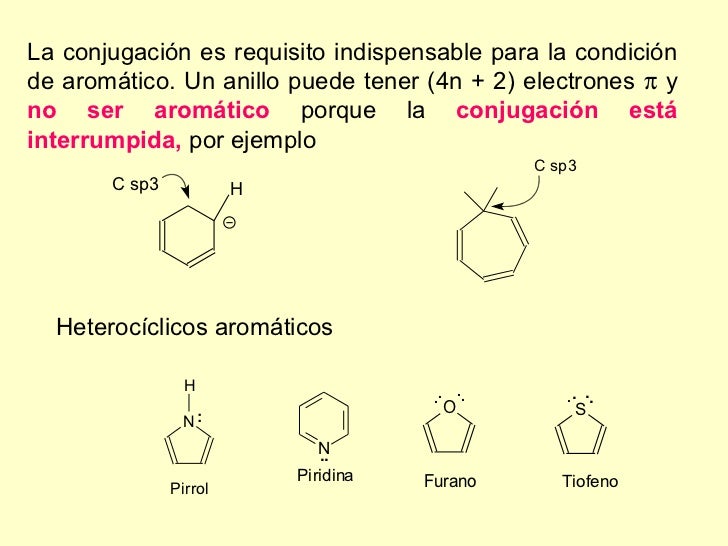
Sistemas aromáticos heterocíclicos
Se llama compuestos heterocíclicos a aquellos que, además de carbono e hidrógeno, poseen al menos un átomo de otro elemento (denominado heteroátomo) formando parte del anillo. Los más comunes son los heterociclos con anillos de 5 o 6 átomos y donde uno o más átomos de carbono están sustituídos por átomos de nitrógeno, oxígeno o azufre. Estos compuestos abundan en la naturaleza y son muy estables: sus anillos están casi libres de tensión.
Se clasifican en dos grupos: alifáticos y aromáticos. Los compuestos alifáticos poseen las propiedades físicas y químicas típicas del heteroátomo específico que incorporan. Por ejemplo
En los heterociclos aromáticos un orbital p del heteroátomo contiene uno o dos (según el caso) electrones no compartidos que se superponen con los orbitales p de los átomos de carbono formando una nube de 6 electrones π por encima y debajo del anillo. Ejemplos:
Nomenclatura

Regla 2. En bencenos disustituidos se indica la posición de los radicales mediante los prefijos orto- (o-), meta (m-) y para (p-). También pueden emplearse los localizadores 1,2-, 1,3- y 1,4-.
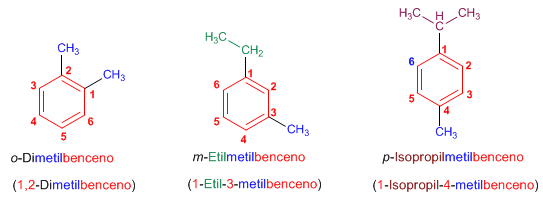
Regla 3. En bencenos con más de dos sustituyentes, se numera el anillo de modo que los sustituyentes tomen los menores localizadores. Si varias numeraciones dan los mismos localizadores se da preferencia al orden alfabético.
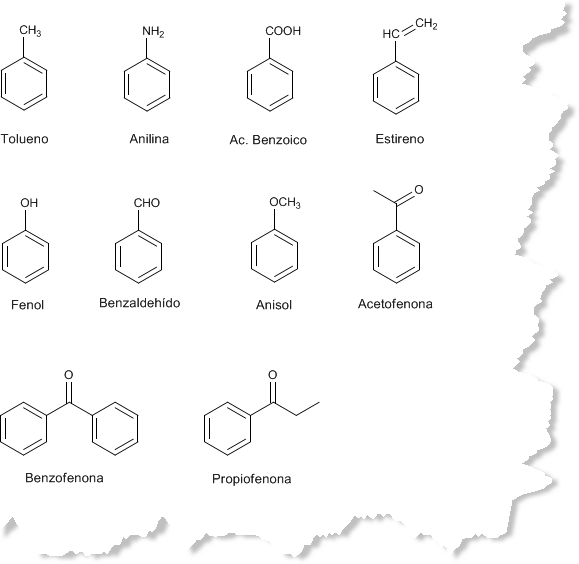
Regla 4. Existen numerosos derivados del benceno con nombres comunes que conviene saber:
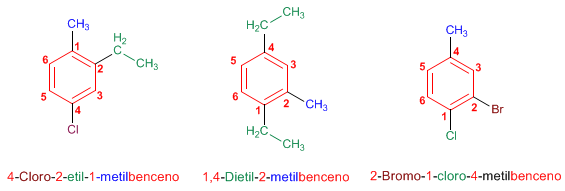
Para nombrar a este tipo de compuestos se indica el número de posición de los sustituyentes, seguido del nombre del sustituyente y seguido del nombre del compuesto. El orden de numeración de estos compuestos es estricta, no se puede alterar y por ende tienen nombres específicos.
Con este video te puedes apoyar de mejor manera para entender las Reglas de Nomenclatura:Nomenclatura Orgánica: Hidrocarburos Aromaticos,HIDROCARBUROS CÍCLICOS. Formulación orgánica. y Hidrocarburos AROMÁTICOS (derivados del benceno). Formulación orgánica.
A continuación se encontraran unos ejercicios para practicar de mejor manera la Nomenclatura
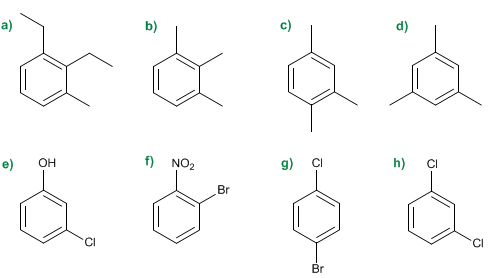

 |
Gracias por Visitarnos ❤ |

Buena actualización del blog
ResponderBorrar