La Química Orgánica
La Química Orgánica es la rama de la química en la que se estudian los compuestos del carbono y sus reacciones. Existe una amplia gama de sustancias (medicamentos, vitaminas, plásticos, fibras sintéticas y naturales, hidratos de carbono, proteínas y grasas) formadas por moléculas orgánicas. Los químicos orgánicos determinan la estructura y funciones de las moléculas, estudian sus reacciones y desarrollan procedimientos para sintetizar compuestos de interés para mejorar la calidad de vida de las personas.
El carbono puede formar enlaces covalentes consigo mismo y con otros elementos para crear una alucinante variedad de estructuras. En química orgánica, aprenderemos acerca de las reacciones químicas usadas para sintetizar locas estructuras basadas en carbono, así como los métodos analíticos para caracterizarlas. También reflexionaremos sobre cómo estas reacciones ocurren a nivel molecular con mecanismos de reacción.
La característica principal que tiene el átomo de carbono y que no tiene el
resto de los elementos químicos, o lo poseen escasamente como es el caso
del silicio, es la concatenación, es decir, la facultad de enlazarse o unirse
consigo mismo formando grandes cadenas o anillos muy estables. Esta propiedad conduce a un número casi infinito de compuestos de carbono, siendo
los más comunes los que contienen carbono e hidrógeno. Esto se debe a que
el carbono puede formar como máximo cuatro enlaces, lo que se denomina
tetravalencia
APLICACIONES DE LA QUÍMICA
ORGÁNICA
BIOQUÍMICA
COMBUSTIBLES
PLÁSTICOS
PEGAMENTOS
MEDICAMENTOS
PINTURAS
ALIMENTOS
FERTILIZANTES
COLORANTES
BEBIDAS
PERFUMES
POLÍMEROS
ALCOHOLES
DESINFECTANTES
COSMETICOS
PESTICIDAS
TEXTILES
ÁTOMO DEL CARBONO
CARBONO
Es el elemento responsable de
la gran complejidad de la
materia orgánica y de que la
misma sea adecuada para
conformar la estructura de
organismos vivientes.
Los átomos de carbono, tienen mucha facilidad para unirse entre sí y formar cadenas
muy variadas. Todos sus átomos forman siempre cuatro enlaces covalentes
Utilizando los enlaces se forman las cadenas carbonadas y es a sucesión de átomos de carbonos entrelazados entre si. Las cadenas carbonadas pueden tener desde 2 hasta varios centenares de átomos de carbono
unidos mediante enlaces simples, dobles, triples y en distintas posiciones.
CADENAS ABIERTAS O ACÍCLICAS:
Es cuando las cadenas presentan dos extremos (Son continuas)
•Cadenas Lineales:
los átomos de carbono pueden escribirse en línea recta.
están constituidas por dos o más cadenas lineales enlazadas. La cadena lineal más importante se denomina cadena principal; las cadenas que se enlazan con ella se llaman radicales.
CADENAS CERRADAS CÍCLICAS:
Son hidrocarburos de cadenas carbonadas cerradas, formadas al unirse dos átomos terminales de una cadena lineal. Las cadenas carbonadas cerradas reciben el nombre de ciclos.•Isociclicos:
son las que solo están formadas por atomos de carbono como por atomos de otros elementos.
Las isociclicas se clasifican en alicíclicas que solo poseen enlaces sencillos y aromáticos que poseen enlaces sencillos y dobles enlaces alternados.
•Cadenas Heterocíclicas:
Se forman cuando por lo menos uno de los átomos de carbono del anillo se encuentra átomos de carbono del anillo se encuentra sustituido por otro elemento, generalmente sustituido por otro elemento, generalmente oxígeno, nitrógeno o azufre.oxígeno, nitrógeno o azufre.CONFIGURACIÓN ELECTRÓNICA DEL CARBONO
1S2 2S2 2P2
Electrones que le faltan para configuración de gas noble= 4
Número de columna = 4
Número de enlaces que puede formar = 4
La química orgánica existe gracias a
las características de la naturaleza
química del carbono:
• Forma cuatro enlaces covalentes
• Al ser el átomo más pequeño de su grupo
forma los enlaces covalentes “más fuertes”
(estables).
• Muchas estructuras posibles, tres geometrías
diferentes
• Puede formar largas cadenas y redes
tridimensionales
• Electronegatividad media (2,55 en la escala
Pauling)
Existen tres alótropos principales del
carbono elemental de los cuales, dos
son naturales (diamante y grafito) y
uno sintético ( fullereno )
Que es un orbital?
Química/Orbitales atómicos. Un orbital atómico es la región del espacio donde se mueven los electrones, los cuales no tienen una trayectoria definida, ya que es imposible conocer la posición de un electrón de un orbital en un momento determinado.


EXCITACIÓN Y HIBRIDACION
La hibridación consiste en una mezcla de orbitales puros en un estado excitado para formar orbitales hibridos equivalentes con orientaciones determinadas en el espacio.
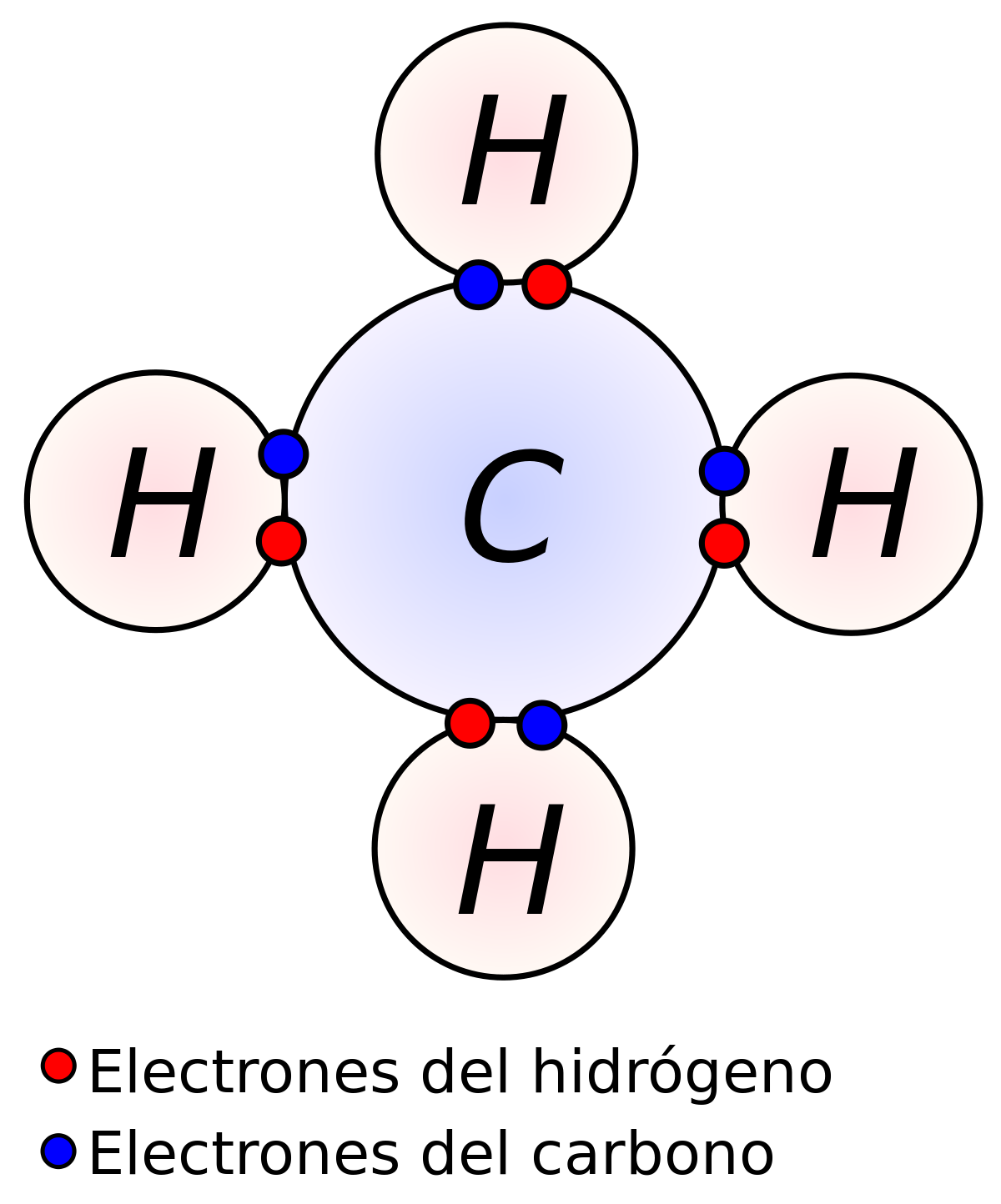
Hibridación sp3 o tetraédrica
Para los compuestos en los cuales el carbono presenta enlaces simples, hidrocarburos saturados o alcanos, se ha podido comprobar que los cuatro enlaces son iguales y que están dispuestos de forma que el núcleo del átomo de carbono ocupa el centro de un tetraedro regular y los enlaces forman ángulos iguales de 109º 28' dirigidos hacia los vértices de un tetraedro. Esta configuración se explica si se considera que los tres orbitales 2p y el orbital 2s se hibridan para formar cuatro orbitales híbridos sp3.Geometría (forma) molecular tetraédrica
Los 4 orbitales sp3 tienen ángulos de 109,5º
entre sí y forman un tetraedro.
ENLACE C-C, HIBRIDACIÓN DE ORBITALES
Geometría (forma) molecular triangular plana
→Los 3 orbitales sp2 están en el mismo plano con ángulos de 120º
entre sí y formando un triangulo.
→El orbital p restante se sitúa perpendicular a este plano.Orbitales híbridos sp:
sp sp
p
p
Geometría (forma) molecular lineal
→Los 2 orbitales sp están alineados (180º).
→Los 2 orbitales p restantes se sitúa perpendiculares a esta línea.Las formas de las moléculas enlazadas por orbitales híbridos está
determinada por los por los ángulos entre estos orbitales:
o Hibridación sp: forma lineal con ángulos de 180° (ej: etino C2H2
)
o Hibridación sp²: forma trigonal (triángulo) plana con ángulos de
120°. Por ejemplo: BCl3
, eteno (C2H4
)?.
o Hibridación sp³: forma tetraédrica con ángulos de 109.5°. Por
ejemplo CCl4
, Metano (CH4
)?.

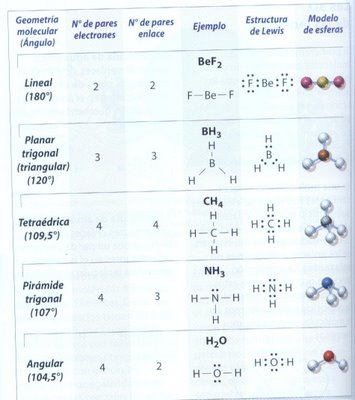
El tipo de hibridación determina la geometría molecular la cual se
resume en el siguiente cuadro:
- Geometría molecular tetraédrica.- El carbono se
encuentra en el centro de un tetraedro y los
enlaces se dirigen hacia los vértices.
- Geometría triangular plana.- El carbono se
encuentra en el centro de un triángulo. Se forma
un doble enlace y dos enlaces sencillos.
- Geometría lineal.- Se forman dos enlaces
sencillos y uno triple.
ENLACE COVALENTE DEL CARBONO
Los compuestos orgánicos están formados por enlaces covalentes
Orbitales moleculares que son orbitales que dejan de pertenecer a un solo núcleo para pasar a depender de dos o más núcleos. El tratamiento matemático que utiliza la Mecánica Cuántica para el cálculo de los orbitales moleculares es el método de la combinación lineal de orbitales atómicos, o método CLOA, que considera que el orbital molecular, y, es el resultado de la combinación lineal, es decir, una suma o una resta, de los dos orbitales atómicos implicados, F1y F2.
TEORIA DE LEWIS
Según Lewis, un ácido era una sustancia química capaz de aceptar un par electrónico, completando así su octeto y por ende logrando estabilidad, mientras que una base era una sustancia química que poseía a lo menos un par electrónico libre (sin enlazar). Como se puede ver, este tipo de definición necesita obligatoriamente un par ácido-base actuando en conjunto, debido a que, por lo general, es imposible dejar electrones libres en un medio cualquiera (salvo con nitrógeno líquido).
El ácido debe tener su octeto de electrones incompleto y la base debe tener algún par de electrones solitario. El amoníaco es una base de Lewis típica y el trifluoruro de boro un ácido de Lewis típico. La reacción de un ácido con una base de Lewis da como resultado un compuesto de adición. Los ácidos de Lewis tales como el tricloruro de aluminio, el trifluoruro de boro, el cloruro estánnico, el cloruro de cinc y el cloruro de hierro (III) son catalizadores sumamente importantes de ciertas reacciones orgánicas.
De esta forma se incluyen sustancias que se comportan como ácidos pero no cumplen la definición de Brønsted y Lowry, y suelen ser denominadas ácidos de Lewis. Puesto que el protón, según esta definición, es un ácido de Lewis (tiene vacío el orbital 1s, en donde "alojar" el par de electrones), todos los ácidos de Brønsted-Lowry son también ácidos de Lewis:
:NH3 | + | []H+ | → | NH4+ | | |
:NH3 | + | []AlCl3 | → | H3N-AlCl3 | | |
Base | | Ácido | | | | |
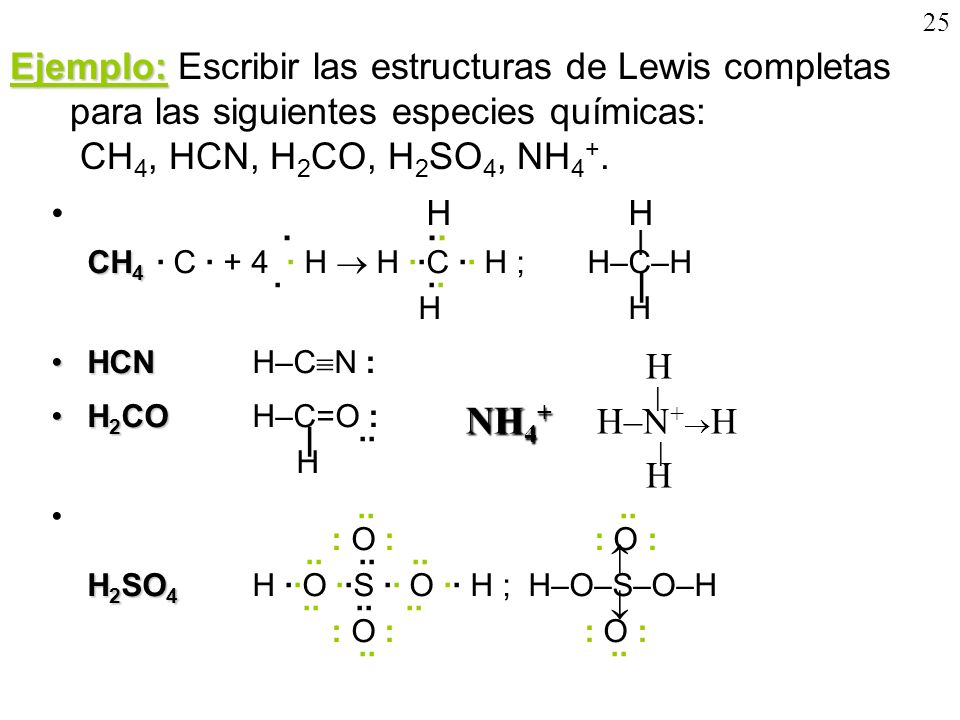 ENTRE LAS REGLAS QUE SE DEBEN DE TOMAR EN CUENTA PARA LA ESTRUCTURA DE LEWIS SON:
ENTRE LAS REGLAS QUE SE DEBEN DE TOMAR EN CUENTA PARA LA ESTRUCTURA DE LEWIS SON:
En el establecimiento de las estructuras de Lewis
es muy importante tener en cuenta tres aspectos
1.- Asignar cargas formales a los átomos
2.- Valorar la existencia de formas resonantes
3.- Hay átomos que no cumplen la regla del
octeto
Resonancia
No siempre existe una única estructura de Lewis que pueda
explicar las propiedades de una molécula o ión.
A cada una de ellas se le denomina forma
resonante y al conjunto híbrido de resonancia
Condiciones para escribir formas resonantes:
1. Para pasar de una forma resonante a otra solamente puedo
mover electrones, nunca átomos.
2. Todas las estructuras resonantes que yo escriba deben ser
estructuras de Lewis válidas.
3. Las estructuras resonantes deben poseer el mismo número de
electrones desapareados.
4. Las estructuras resonantes más importantes son las de menor
energía potencial.
Pero cabe mencionar tambien que hay incumplimientos de la regla del
octeto
- Elementos del tercer periodo como el fósforo se rodean de 10 electrones
- Los átomos con número impar de electrones suelen incumplir la regla
GRACIAS POR VISITARNOS .....❤














Buena presentación de la información y la estructura de las unidades
ResponderBorrar