- -La fórmula que les define es CnH2n+2. En este caso, hay que exponer que la n corresponde al número de carbonos que tiene.
- -A la hora de proceder a denominar los alcanos se realiza usando el citado sufijo “-ano” y un prefijo. Este puede ser de diferentes tipos, tales como los siguientes: “met-”, “but-”, “et-”, “prop-”… Ejemplos de esto son metano, propano, butano, etano…
- -De los alcanos se puede decir que son insolubles en el agua.
- -El principal uso que se les suele dar es como combustibles. ¿Por qué? Porque, de manera incuestionable, liberan una gran cantidad de calor.
- -Por regla general, los alcanos se dividen en cuatro grupos diferenciados: cíclicos, lineales, policíclicos y ramificados.
- -Sus puntos de ebullición y también de fusión son bajos.
- -No son rígidos.
En el sistema IUPAC de nomenclatura un nombre está formado por tres partes: prefijos, principal y sufijos; Los prefijos indican los sustituyentes de la molécula; el sufijo indica el grupo funcional de la molécula; y la parte principal el número de carbonos que posee. Los alcanos se pueden nombrar siguiendo siete etapas:
Regla 1.- Determinar el número de carbonos de la cadena más larga, llamada cadena principal del alcano. Obsérvese en las figuras que no siempre es la cadena horizontal.
El nombre del alcano se termina en el nombre de la cadena principal (octano) y va precedido por los sustituyentes.
Regla 2.- Los sustituyentes se nombran cambiando la terminación –ano del alcano del cual derivan por –ilo (metilo, etilo, propilo, butilo). En el nombre del alcano, los sustituyentes preceden al nombre de la cadena principal y se acompañan de un localizador que indica su posición dentro de la cadena principal. La numeración de la cadena principal se realiza de modo que al sustituyente se le asigne el localizador más bajo posible.
Regla 3.- Si tenemos varios sustituyentes se ordenan alfabéticamente precedidos por lo localizadores. La numeración de la cadena principal se realiza para que los sustituyentes en conjunto tomen los menores localizadores.
Si varios sustituyentes son iguales, se emplean los prefijos di, tri, tetra, penta, hexa, para indicar el número de veces que aparece cada sustituyente en la molécula. Los localizadores se separan por comas y debe haber tantos como sustituyentes.
Los prefijos de cantidad no se tienen en cuenta al ordenar alfabéticamente.
Regla 4.- Si al numerar la cadena principal por ambos extremos, nos encontramos a la misma distancia con los primeros sustituyentes, nos fijamos en los demás sustituyentes y numeramos para que tomen los menores localizadores.
Regla 5.- Si al numerar en ambas direcciones se obtienen los mismos localizadores, se asigna el localizador más bajo al sustituyente que va primero en el orden alfabético.
Regla 6.- Si dos a más cadenas tienen igual longitud, se toma como principal la que tiene mayor número de sustituyentes.
Regla 7.- Existen algunos sustituyentes con nombres comunes aceptados por la IUPAC, aunque se recomienda el uso de la nomenclatura sistemática.
Los nombres sistemáticos de estos sustituyentes se obtienen numerando la cadena comenzando por el carbono que se une a la principal. El nombre del sustituyente se forma con el nombre de la cadena más larga terminada en –ilo, anteponiendo los nombres de los sustituyentes que tenga dicha cadena secundaria ordenados alfabéticamente. Veamos un ejemplo:
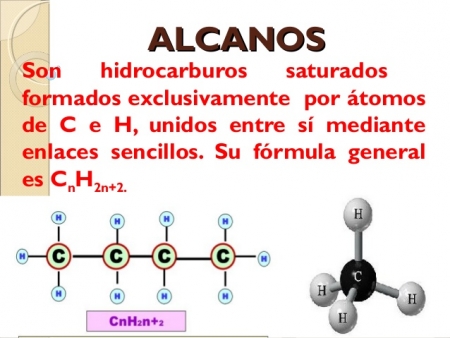
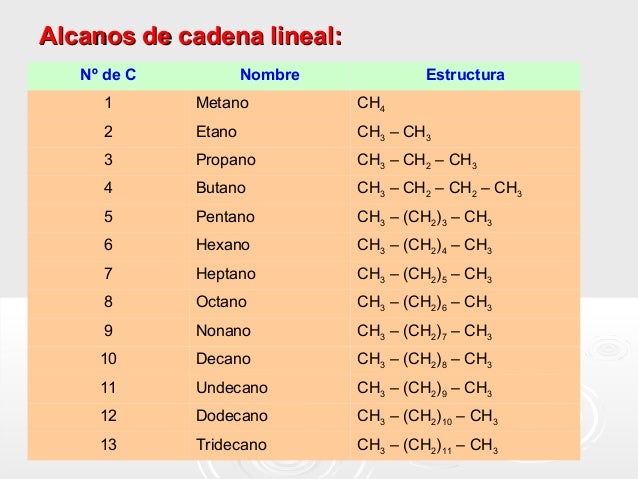
Los hidrocarburos alifáticos saturados responden a la fórmula general CnH2n+2 , donde n es el número de átomos de carbono. Se nombran según el número de átomos de carbono de la cadena, terminados en -ano.
- CH4 metano CH3?CH3 etano
- CH3?CH2?CH3 propano
- CH3?CH2?CH2?CH3 butano
- CH3?CH2?CH2?CH2?CH3 pentano
Los compuestos, como los de arriba, con el mismo grupo funcional pero distinto número de átomos de carbono en la cadena, forman una serie homóloga.
Cuando el hidrocarburo pierde un hidrógeno, queda un radical. Éste recibe la misma denominación que el hidrocarburo del que procede, pero terminado en -ilo, si se dice el nombre aislado, y en -il, si se dice formando parte de un compuesto:
- CH3? metilo
- CH3?CH2? etilo
- CH3?CH2?CH2? propilo
Cuando los hidrocarburos son de cadena ramificada, se nombran de la siguiente forma:
- Se toma como base la cadena más larga.
- Se numeran los carbonos comenzando por el extremo que tiene más cerca una rama, nombrándose éstas por orden alfabético precedidas del número que indica el carbono en el que se ha efectuado la sustitución. Las ramas se consideran como radicales unidos a la cadena principal.
- Se nombran en primer lugar los radicales, precedidos del número del carbono al que están unidos.
Las principales propiedades de los hidrocarburos saturados son:
- Los puntos de fusión y ebullición aumentan con el número de átomos de carbono. Los valores más bajos corresponden a los hidrocarburos de cadena ramificada.

- Combustión: es la reacción más importante. Es el fundamento del uso de los hidrocarburos como combustibles al desprender una gran cantidad de energía. En todos los casos se desprende dióxido de carbono y agua. La reacción del butano es:
2 C4H10 + 13 O2 ® 8 CO2 + 10 H2O + 2.640 kJ/mol
- Craqueo: es la descomposición de los hidrocarburos en otros hidrocarburos de menor número de átomos de carbono. Cuando se realiza con calor se denomina craqueo térmico. Si tiene lugar mediante catalizadores es el craqueo catalítico. Esta reacción se utiliza para obtener gasolinas a partir de otras fracciones petrolíferas más pesadas.
- Halogenación: procede de sustituir un hidrógeno del hidrocarburo por un halógeno. Para ello hay que irradiar adecuadamente la mezcla hidrocarburo-halógeno. La reacción transcurre mediante radicales libres

Por cada anillo que posea un compuesto, su fórmula empírica pierde 2H respecto del alcano no cíclico.
Regla 1. El nombre del cicloalcano se construye a partir del nombre del alcano con igual número de carbonos añadiéndole el prefijo ciclo-.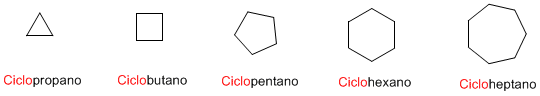
Regla 2. En cicloalcanos con un solo sustituyente, se toma el ciclo como cadena principal de la molécu-la. Es innecesaria la numeración del ciclo.
Regla 3. Si el cicloalcano tiene dos sustituyentes, se nombran por orden alfabético. Se numera el ciclo comenzando por el sustituyente que va antes en el nombre.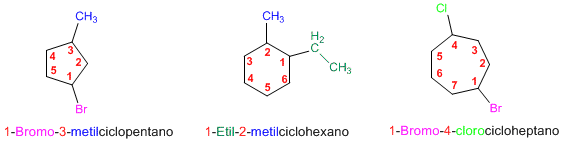
Regla 4. Si el anillo tiene tres o más sustituyentes, se nombran por orden alfabético. La numeración del ciclo se hace de forma que se otorguen los localizadores más bajos a los sustituyentes.
Nomenclatura Orgánica Básica: Alcanos
- 1. Nomenclatura Orgánica Básica Hidrocarburos Alifáticos. Alcanos y Cicloalcanos
- 2. Hidrocarburos - Clasificación Los hidrocarburos son compuestos formados exclusivamente por átomos de carbono e hidrógeno a través de enlaces covalentes. Se dividen en Alifáticos y Aromáticos. Los primeros se subdividen a su vez en Alcanos, Alquenos, Alquinos y sus análogos Cíclicos, también denominados Alicíclicos
- 3. Nomenclatura de Alcanos Los alcanos se nombran con la terminación “ano” y los cuatro primeros compuestos de la serie reciben los nombres de Metano, Etano, Propano y Butano. A partir de cinco átomos de carbono los nombres se derivan del prefijo griego o latino (penta, hexa, hepta, octa, nona, deca, undeca, etc.) para el número particular de carbonos en el compuesto, resultando así: pentano, hexano, heptano, etc.
- 4. El átomo de Carbono Cuando observamos moléculas como la del metano, CH4, nos damos cuenta que estas no podrían formarse ya que el carbono solo posee dos orbitales con un electrón y se precisan cuatro para formar los cuatro enlaces de la molécula
- 5. Esta dificultad puede ser resuelta considerando para el Carbono un estado excitado en el que uno de los electrones del orbital 2s pase a ocupar el orbital 2pz vacío. Se obtienen 4 orbitales híbridos sp3 y el enlace ahora es posible
- 6. Los Alcanos solo contienen átomos de Carbono e Hidrógeno en su molécula, unidos entre sí por enlaces covalentes sencillos A continuación se muestra una tabla con algunos de los miembros de esta serie:
- 7. Los Alcanos pueden ser:
- 8. En los alcanos de cadena abierta, lineales o normales, tan solo existen carbonos primarios (extremos de la cadena) y secundarios (intermedios), mientras que en los ramificados pueden haber carbonos primarios, secundarios, terciarios y cuaternarios, dependiendo de si están unidos a uno, dos, tres o cuatro átomos de carbono.
- 9. Identifique el grado de substitución de cada átomo de carbono en las siguientes moléculas:
- 10. Note que podemos escribir sus formulas de diferentes maneras:
- 11. Alcanos Acíclicos Ramificados Presentan ramificaciones o cadenas laterales que también se denominan radicales. Un radical es un conjunto de átomos que resulta de la pérdida formal de un átomo de H de un hidrocarburo. Si el hidrocarburo es un alcano, el radical resultante se denomina radical alquilo y se nombra sustituyendo la terminación -ano por -ilo:
- 12. Algunos ejemplos de radicales son:
- 13. Antes de estudiar las etapas para nombrar correctamente un alcano, será importante poder escribir todos los isómeros correspondientes a una fórmula molecular
- 14. Isómeros Los Isómeros son compuestos diferentes que comparten la misma fórmula molecular
- 15. • Todos los isómeros estructurales deben corresponder a la misma fórmula molecular. Evite escribir estructuras duplicadas. Por ejemplo si desea escribir los isómeros del heptano C7H16, siga las siguientes etapas: .- Empiece con la estructura de cadena lineal de siete carbonos, para la cual solo hay una posible: CH3-CH2-CH2-CH2-CH2-CH2-CH3
- 16. • Considere los isómeros mas próximos con una cadena continua de seis carbonos, donde un grupo o radical CH3 deberá estar unido a uno de los átomos de carbono no terminales para producir estructuras de cadena ramificada:
- 17. Los Isómeros del n- Hexano, escritos como cadenas un poco mas detalladas, son los siguientes:
- 18. Vamos a nombrar el siguiente alcano: Ubicamos la cadena de carbonos continua más larga y numeramos por el extremo más cercano al radical, e identificamos los que están presentes:
- 19. La cadena continua más larga tiene 7 carbonos y se empezó la numeración por el extremo derecho porque es el más cercano a un radical. Identificamos los radicales y el número del carbono al que están unidos, los acomodamos en orden alfabético y unido el último radical al nombre de la cadena. 4-ETIL-2-METILHEPTANO
- 20. Otro ejemplo: Buscamos la cadena continua más larga, la cual no tiene que ser siempre horizontal. Numeramos por el extremo más cercano al radical. Ordenamos los radicales en orden alfabético y unimos el nombre de la cadena al último radical.
- 21. 5-ISOPROPIL-3- METILNONANO
- 22. Nombre el siguiente alcano: 5-n –BUTIL-4,7-DIETILDECANO
- 23. 3-ETIL-4-METILHEXANO
- 24. Ahora, el caso contrario. Partiendo del nombre, escribir la formula estructural…
- 25. Escribir la formula de: 3,4,6-TRIMETIL HEPTANO 1.- La cadena heptano tiene 7 átomos de carbono. Los numeramos de izquierda a derecha, pero se puede hacer de derecha a izquierda
- 26. Ahora, se colocan los radicales en el carbono que corresponda, teniendo cuidado de colocar el radical por el enlace libre. CH2
- 27. Completamos la estructura con los hidrógenos necesarios
- 28. 3-METIL-5-ISOPROPILNONANO El Nonano es una cadena de 9 carbonos Colocamos los radicales:
- 29. Los radicales pueden acomodarse de diferentes formas, siempre y cuando conserve su estructura. Finalmente completamos con los hidrógenos necesarios para que cada carbono tenga sus 4 enlaces.
- 30. 5-TER-BUTIL-5-ETILDECANO El Decano es una cadena de 10 carbonos Los dos radicales de la estructura están en el mismo carbono por lo tanto se coloca uno arriba y el otro abajo del carbono # 5:
- 31. Completamos con los hidrógenos:
- 32. 5-SEC-BUTIL-5-TER-BUTIL-8-METILNONANO Nonano es una cadena de 9 carbonos: Colocamos los radicales:
- 33. Ahora completamos con hidrógeno para que cada carbono tenga 4 enlaces:
- 34. Un último ejemplo: 5-ISOBUTIL-4-ISOPROPIL-6-n-PROPILDECANO Decano es una cadena de 10 carbonos que numeramos de izquierda derecha:
- 35. Colocamos los radicales cuidando de acomodarlos en forma correcta
- 36. Contamos los enlaces para poner los hidrógenos necesarios para completar 4 enlaces a cada carbono:
- 37. CICLOALCANOS Muchos compuestos orgánicos son cíclicos: es decir sus átomos están formando un anillo. Su fórmula general es (CH2)n y se suelen representar como polígonos. Se nombran como los alcanos acíclicos, anteponiendo el prefijo “ciclo”
- 38. Los Cicloalcanos sustituidos se nombran tomando como base el nombre de Cicloalcanos y nombrando los grupos alquilo como sustituyentes siguiendo las reglas de la IUPAC. Si un ciclo va como sustituyente se nombra como cicloalquilo.
- 39. Los cicloalcanos sustituidos a diferencia de los alcanos de cadena abierta, pueden presentar isomería geométrica, debido a que los enlaces simples C-C no tienen libre rotación. Pueden existir cicloalcanos cis y cicloalcanos trans.
- 40. Los nombres de los cicloalcanos sin cadenas laterales se forman anteponiendo el prefijo "ciclo" al nombre del alcano lineal correspondiente con el mismo número de átomos de carbono. Su estructura se representa con un polígono correspondiente con su número de carbonos:
- 41. Los sustituyentes univalentes derivados de cicloalcanos sin cadenas laterales se nombran reemplazando la terminación "-ano" del nombre del hidrocarburo por la terminación "- il"; el átomo de carbono con la valencia libre se numera como 1. El nombre genérico de estos sustituyentes es "cicloalquilo".

Los compuestos que contienen carbono e hidrógeno sólo se denominan hidrocarburos. Los alcanos contienen enlaces sencillos C-H y se dice que están saturados, los alquenos poseen enlaces dobles C-C y los alquinos tienen enlaces triples C-C. El término hidrocarburo aromático se utiliza frecuentemente para indicar la presencia de un anillo de benceno.
Proyecciones de Newman del butano.
Las rotaciones alrededor del enlace central del butano dan lugar a disposiciones moleculares diferentes. Tres de esas conformaciones tienen nombres específicos.
Para el butano existen dos conformaciones alternadas diferentes: gauche y anti. La conformación gauche tiene un ángulo diedro de 60º entre los grupos metilo, mientras que la conformación anti tiene un ángulo diedro de 180º entre los grupos metilo. Hay una conformación distinta cuando el ángulo diedro entre los grupos metilo es 0º, esta conformación se denomina totalmente eclipsada
Isomería cis-trans en los alcanos
Como en los alquenos, en los anillos de cicloalcanos está restringida la libre rotación. Dos sustituyentes en un cicloalcano pueden estar al mismo lado (cis) o en lados opuestos (trans) del anillo.
Tensión de anillo en el ciclopropano
Los ángulos de enlace se han comprimido hasta 60º, en lugar de 109,5º de los ángulos de enlace correspondientes a la hibridación sp3 de los átomos de carbono. Esta severa tensión angular da lugar a un solapamiento no lineal de los orbitales sp3 y forma «enlaces torcidos
Todos los enlaces carbono-carbono están eclipsados, generando una tensión torsional que contribuye a la tensión total del anillo.
La tensión angular y la tensión torsional en el ciclopropano hacen que el tamaño de este anillo sea extremadamente reactivo.
La conformación del ciclobutano es tal que el anillo está ligeramente doblado. Esta deformación de la coplanaridad proporciona un relajamiento parcial del eclipsamiento de los enlaces, como se observa en la proyección de Newman. Compare esta estructura real con la hipotética estructura plana
Un compuesto cíclico con 4 o más átomos de carbono adopta conformaciones que no son planas para relajar la tensión del anillo. El ciclobutano adopta la conformación doblada para disminuir la tensión torsional causada al eclipsar los átomos de hidrógeno.
CONFORMACIONES DEL CICLOPENTANO
La conformación del ciclopentano está ligeramente doblada, como la forma de un sobre. Esta conformación plegada reduce el eclipsamiento de los grupos CH2 adyacentes
Conformación de bote del ciclohexano
La conformación de barca simétrica del ciclohexano, el eclipsamiento de los enlaces da lugar a tensión torsional. En la molécula representada, la barca se retuerce y se forma la barca torcida, una conformación con los enlaces menos eclipsados y con menor interacción entre los dos hidrógenos mástil.
Conformación de silla del ciclohexano
Los enlaces axiales se dirigen verticalmente y de forma paralela al eje del anillo. Los enlaces ecuatoriales se dirigen hacia fuera, hacia el «ecuador» del anillo. Tal como se numeran los carbonos en la figura, en los carbonos impares los enlaces dirigidos verticalmente y hacia arriba son axiales y los enlaces dirigidos hacia abajo, pero en un plano ecuatorial, son ecuatoriales. En los carbonos pares, los enlaces dirigidos verticalmente y hacia abajo son axiales, y los enlaces dirigidos hacia arriba y en un plano ecuatorial son ecuatoriales
Proyección de Newman del metilciclohexano: metilo axial.
cuando el sustituyente metilo está en posición axial en C1, está en disposición gauche respecto a C3. (b) El grupo metilo axial en C1 también adopta una relación gauche respecto a C5 del anillo.En la proyección de Newman resulta más fácil observar la interacción estérica entre el sustituyente metilo y los hidrógenos y carbonos del anillo.
Gracias por visitarnos

No hay comentarios.:
Publicar un comentario